
Borréliose de Lyme et maladies vectorielles à tiques
Les maladies vectorielles à tiques sont transmises lors de la piqûre de la tique. L’être humain n’est qu’un hôte accidentel pour que la tique fasse son repas de sang.
La borréliose de Lyme est transmise à l’être humain par la piqûre de certaines tiques, principalement du genre Ixodes.
D’autres arthropodes (moustiques, puces, poux, taons) peuvent être vecteurs d’autres maladies infectieuses. Ces infections sont regroupées sous le terme général de maladies vectorielles, car elles sont transmises par des vecteurs biologiques.
Il est important de ne pas confondre ces différentes pathologies, dont les modes de transmission et les agents responsables sont distincts.
Une transmission materno-fœtale transplacentaire de certaines infections transmises par les tiques a été rapportée dans la littérature scientifique. Elle demeure rare et fait l’objet d’une surveillance particulière en cas d’infection aiguë pendant la grossesse. Un traitement adapté réduit le risque de transmission.
À ce jour, aucune transmission transfusionnelle de la borréliose de Lyme n’a été formellement documentée. En revanche, la transmission transfusionnelle de certains autres agents infectieux transmis par les tiques, notamment Babesia, est reconnue, notamment aux Etats-Unis.
Il est officiellement reconnu qu’en France existent des co-infections
En France, Ixodes ricinus peut transmettre à l’être humain plusieurs agents infectieux, notamment des bactéries telles que Anaplasma phagocytophilum ou certaines espèces de Rickettsia, des virus comme le virus de l’encéphalite à tiques, ainsi que des parasites du genre Babesia. D’autres agents infectieux ont été détectés chez les tiques, mais leur rôle exact dans la transmission à l’homme peut varier selon les contextes épidémiologiques.
(HCSP – Haut Conseil de la Santé Publique 2010)
Les maladies transmises par les tiques
Les maladies transmises par les tiques regroupent plusieurs agents infectieux, dont la répartition peut varier selon les régions et les écosystèmes.
La borréliose de Lyme est due à des bactéries du complexe Borrelia burgdorferi sensu lato.
En Amérique du Nord, l’espèce principalement impliquée est Borrelia burgdorferi sensu stricto. En Europe, on retrouve également Borrelia burgdorferi sensu stricto, mais d’autres espèces du même complexe sont plus fréquemment rencontrées, notamment Borrelia afzelii et Borrelia garinii.
Les tests sérologiques utilisés en France sont conçus pour détecter des anticorps dirigés contre plusieurs espèces européennes du complexe Borrelia burgdorferi sensu lato. Comme tout examen biologique, leur interprétation doit tenir compte du contexte clinique et du stade de la maladie.
Le diagnostic des maladies transmises par les tiques repose avant tout sur l’évaluation clinique réalisée par un médecin, en tenant compte des symptômes, du contexte d’exposition et de l’examen médical.
Les examens biologiques constituent des outils complémentaires d’aide au diagnostic. Leur interprétation doit être intégrée à l’ensemble des données cliniques.
Parmi les agents infectieux transmis par les tiques figurent notamment :
– La borréliose de Lyme (complexe Borrelia burgdorferi sensu lato)
– L’anaplasmose et l’ehrlichiose
– Les rickettsioses
– La babésiose
– La tularémie
– L’encéphalite à tiques (méningo-encéphalite virale)
– La fièvre hémorragique de Crimée-Congo (présente dans certaines régions du monde)
D’autres agents infectieux, plus rares ou émergents selon les zones géographiques, ont également été identifiés, tels que le virus Powassan en Amérique du Nord ou le virus Alongshan en Asie.
Certaines pathologies associées aux piqûres de tiques, comme le syndrome d’allergie à l’alpha-gal (allergie retardée à la viande rouge), font actuellement l’objet de travaux de recherche.
1. La borreliose de Lyme
La borréliose de Lyme (ou maladie de Lyme) est une maladie infectieuse d’origine bactérienne transmise à l’être humain par la piqûre de certaines tiques. Elle appartient à la catégorie des maladies vectorielles à tiques.
Les bactéries responsables sont des spirochètes du genre Borrelia. En Europe, plusieurs espèces du complexe Borrelia burgdorferi sensu lato sont impliquées, notamment B. garinii, B. afzelii, B. burgdorferi sensu stricto, B. bavariensis et B. spielmanii.
En climat tempéré, la transmission survient principalement lors d’activités en plein air, du printemps à l’automne, périodes d’activité accrue des tiques.
La période d’incubation est le plus souvent comprise entre 3 et 30 jours après la piqûre.
Le premier signe clinique est généralement un érythème migrant, une plaque rouge qui s’étend progressivement autour du point de piqûre.
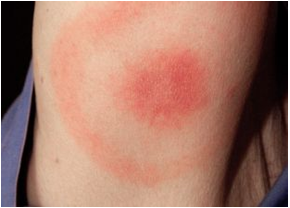
D’autres symptômes peuvent apparaître selon la phase d’évolution : fatigue, fièvre modérée, douleurs articulaires ou musculaires, atteintes neurologiques ou cardiaques dans les formes disséminées.
L’évolution clinique varie selon les individus et toutes les phases ne sont pas systématiquement observées.
Classiquement décrite en différentes phases évolutives (localisée, disséminée précoce et disséminée tardive), la maladie peut, dans certains cas, être suivie de symptômes persistants après un traitement conforme aux recommandations. Cette situation est désignée sous le terme de syndrome post-traitement de la borréliose de Lyme (PTLDS) dans les recommandations de la HAS.
En France, l’incidence annuelle estimée de la borréliose de Lyme est du même ordre de grandeur que celle du cancer du sein, et nettement supérieure au nombre annuel de nouveaux diagnostics d’infection par le VIH. Ces comparaisons reposent sur les données officielles de surveillance sanitaire.
Pr Trouillas
Les bactéries du complexe Borrelia burgdorferi sensu lato présentent une grande diversité génétique. Des travaux récents suggèrent que certaines souches pourraient être mieux adaptées à certains hôtes, ce qui pourrait influencer leur circulation dans l’environnement.
La prise en charge des formes persistantes de la maladie a fait l’objet de débats scientifiques ces dernières années. Jusqu’à la reconnaissance officielle du syndrome post-traitement de la borréliose de Lyme (PTLDS) par la Haute Autorité de Santé en 2025, de nombreux patients ont exprimé un sentiment de manque de reconnaissance de leurs symptômes persistants et des difficultés dans leur parcours de soins. France Lyme se félicite de cette avancée majeure, qui répond à une attente ancienne et qui avait motivé la création de l’association en 2008. Il convient désormais de poursuivre les efforts en matière de recherche thérapeutique et d’améliorer l’accueil et la prise en charge des patients au sein des centres spécialisés.
À ce jour, il n’existe pas de vaccin contre la borréliose de Lyme disponible en France. En revanche, un vaccin contre l’encéphalite à tiques est commercialisé dans les zones concernées. Des recherches vaccinales sont en cours concernant la maladie de Lyme.
Certaines maladies transmises par les tiques peuvent être reconnues au titre des maladies professionnelles, selon les conditions d’exposition et la réglementation en vigueur.
Les différentes formes de la borréliose de Lyme :
La borréliose de Lyme évolue classiquement en plusieurs phases cliniques, bien que toutes ne soient pas systématiquement observées chez chaque patient.
La phase précoce localisée se manifeste le plus souvent par un érythème migrant, une rougeur cutanée s’étendant progressivement autour du point de piqûre.
En l’absence de traitement ou parfois malgré un traitement adapté, la maladie peut évoluer vers une phase disséminée précoce, au cours de laquelle la bactérie peut atteindre différents organes, provoquant notamment des atteintes neurologiques (neuroborréliose), articulaires ou cardiaques.
La neuroborréliose peut se traduire par des maux de tête persistants, des troubles de la concentration, des douleurs radiculaires, une paralysie faciale ou d’autres symptômes neurologiques.
Plus tardivement, une phase disséminée tardive peut apparaître, caractérisée principalement par des atteintes articulaires (arthrite de Lyme), mais aussi par des manifestations neurologiques persistantes.
Enfin, certains patients peuvent présenter des symptômes persistants après un traitement conforme aux recommandations ; cette situation est désignée sous le terme de syndrome post-traitement de la borréliose de Lyme (PTLDS) dans les recommandations de la Haute Autorité de Santé, que nous appelons aussi Lyme long, pour plus de compréhension au niveau des patients et du grand public.
L’évolution clinique varie d’une personne à l’autre et justifie une évaluation médicale individualisée.
Toute atteinte neurologique survenant après une exposition possible aux tiques doit conduire à une évaluation médicale attentive, car la neuroborréliose peut se manifester par des symptômes variés et peu spécifiques, parfois confondus avec d’autres affections neurologiques ou fonctionnelles.
https://www.revmed.ch/RMS/2013/RMS-384/Neuroborreliose-meningo-encephalite-verno-estivale-et-neurosyphilis
Concrètement :
- Les symptômes peuvent être non spécifiques : fatigue importante, troubles de la concentration, céphalées diffuses.
- Ils peuvent mimer d’autres pathologies : troubles anxieux, dépression, migraine, sclérose en plaques, neuropathies périphériques, hernie discale en cas de douleurs radiculaires.
- La piqûre de tique peut être passée inaperçue, et l’érythème migrant peut ne pas avoir été observé.
- Les manifestations peuvent apparaître à distance de l’exposition, ce qui complique le lien chronologique.
Facteurs de risque :
Le principal facteur de risque est l’exposition aux tiques dans les zones où elles sont présentes, notamment lors d’activités en milieu forestier, rural ou herbeux.
Le risque dépend de plusieurs éléments :
• la durée d’attachement de la tique
• la densité locale de tiques infectées
• la période d’activité des tiques (principalement du printemps à l’automne en climat tempéré)
• l’absence de retrait rapide de la tique
La majorité des personnes piquées par une tique infectée ne développent pas nécessairement une maladie, mais toute apparition de symptômes après une exposition doit conduire à une évaluation médicale.
Liens annexes :
- Maladie de Lyme chez le cheval
- Host adaptation drives genetic diversity in a vector-borne disease system
2. Les autres borrelia
D’autres espèces du genre Borrelia sont identifiées en Europe, en Afrique et dans d’autres régions du monde, notamment Borrelia miyamotoi et Borrelia crocidurae. Certaines de ces bactéries sont responsables de fièvres récurrentes.
Les borrélioses à fièvres récurrentes regroupent un ensemble d’infections caractérisées par des épisodes fébriles répétés, séparés par des phases d’amélioration transitoire. Elles peuvent être transmises par des tiques ou, selon les espèces concernées, par des poux. Les signes cliniques sont souvent peu spécifiques et d’apparition brutale (fièvre élevée, céphalées, douleurs musculaires).
Publication sur le sujet :
3. La babésiose
La babésiose est une infection parasitaire causée par des protozoaires du genre Babesia, appartenant au phylum des Apicomplexa, comme les Plasmodium responsables du paludisme. Chez les animaux domestiques, notamment le chien et le chat, la maladie est souvent appelée piroplasmose.
Le parasite est transmis aux vertébrés par la piqûre de certaines tiques, principalement du genre Ixodes en Europe. Chez l’être humain, les infections sont le plus souvent dues à Babesia microti (plus fréquente en Amérique du Nord) et à Babesia divergens en Europe.
En France, la babésiose humaine reste probablement sous-diagnostiquée. Sa répartition géographique est hétérogène et dépend de la présence des tiques vectrices, des réservoirs animaux et des conditions écologiques favorables. Chez les animaux, notamment les chiens, la babésiose est fréquemment observée en médecine vétérinaire, avec des variations régionales importantes. Certaines régions, comme le sud-ouest de la France et certaines zones du Massif central, sont considérées comme plus exposées.
Chez les bovins, qui constituent le principal réservoir de Babesia divergens en Europe, l’infection peut être fréquente. Chez l’être humain, après une période d’incubation d’environ une à trois semaines, la maladie peut provoquer une hémolyse (destruction des globules rouges) se traduisant par une fièvre élevée, des frissons, une fatigue importante, des douleurs musculaires et, dans les formes sévères, des urines foncées liées à l’hémoglobinurie. Les formes graves surviennent principalement chez les personnes âgées, splénectomisées (qui ont subi une ablation de la rate) ou immunodéprimées.
Si certaines infections peuvent être paucisymptomatiques (très peu de symptômes) ou asymptomatiques, des cas cliniques sont également décrits chez des personnes immunocompétentes. L’évolution dépend du terrain et une prise en charge médicale adaptée est nécessaire.
Certaines études sérologiques ont mis en évidence des anticorps dirigés contre Babesia divergens chez des personnes exposées aux tiques en France. Toutefois, la détection directe du parasite par des méthodes moléculaires demeure rare dans la population générale.
La Babésiose humaine : bilan de 10 ans d’analyses – 29/05/18 – Doi : 10.1016/j.medmal.2018.04.284 – M. Jouglin, N. De la Cotte, C. Bonsergent, S. Bastian, L. Malandrin INRA/Oniris, Nantes, France https://www.em-consulte.com/article/1217242
La présence d’anticorps traduit un contact immunologique avec l’agent infectieux, sans préjuger nécessairement d’une infection active. Chez les personnes immunocompétentes, l’infection peut être asymptomatique ou spontanément contrôlée par le système immunitaire.
Dans certains contextes cliniques particuliers, notamment chez les patients immunodéprimés, une infection persistante peut survenir et nécessiter une prise en charge spécifique. L’amélioration des techniques diagnostiques contribue à une meilleure identification des infections humaines à Babesia.
Transmission :
La babésiose est principalement transmise à l’être humain par la piqûre de tiques infectées, notamment du genre Ixodes. Le parasite est inoculé lors du repas sanguin de la tique et infecte les globules rouges.
Une transmission par transfusion sanguine est également reconnue, en particulier dans les zones où le parasite circule. De rares cas de transmission materno-fœtale ont été rapportés dans la littérature scientifique.
La babésiose n’est pas considérée comme transmissible d’une personne à une autre par contact direct.
Incubation :
Après une piqûre de tique infectée, la période d’incubation est généralement comprise entre une et trois semaines.
En cas de transmission transfusionnelle, l’incubation peut être plus variable, allant de quelques jours à plusieurs semaines.
Les manifestations cliniques peuvent débuter brutalement par une fièvre élevée, des frissons, une fatigue intense et des douleurs musculaires. Dans les formes plus sévères, une hémolyse (destruction des globules rouges) peut entraîner une anémie et des urines foncées.
Facteurs de risque
Le risque d’infection dépend principalement de l’exposition aux tiques dans les zones où le parasite circule.
Les formes graves de babésiose surviennent plus fréquemment chez :
- les personnes immunodéprimées
- les patients splénectomisés
- les personnes âgées
- les patients présentant des comorbidités chroniques
Chez les personnes immunocompétentes, l’infection peut être asymptomatique ou modérée, bien que des formes cliniques soient également décrites.
Quelques articles scientifiques sur le sujet :
- La Babésiose humaine : bilan de 10 ans d’analyses, 2018
- La babesiose bovine, une zoonose à risque pour l’homme par Marie-Elise Collot, thèse pharmacien
- La babesiose : une maladie à tique émergente >
- Transmission sanguine de la babesia par transfusion >
- Risque de transmission de babesia par transfusion >
- Transmission de babesia par transfusion sanguine >
- Transmission de Babesia Divergens et de Babesia sp.EU1 par les tiques Ixodes Ricinus >
4. Les bartonelloses (maladie de la griffe du chat)
Les bartonelloses sont des infections causées par des bactéries du genre Bartonella. Parmi elles, Bartonella henselae est responsable de la maladie des griffes du chat.
Le principal réservoir de Bartonella henselae est le chat domestique. La transmission à l’être humain se fait le plus souvent par griffure ou morsure, ou par contact de plaies ou de muqueuses avec des sécrétions contaminées. Les puces jouent un rôle important dans la circulation de la bactérie entre chats.
Chez le chat, l’infection est généralement asymptomatique. La proportion de chats porteurs varie selon les régions et les conditions d’exposition aux puces.
À ce jour, la transmission à l’être humain par tiques n’est pas formellement démontrée. Des recherches sont en cours concernant le rôle potentiel d’autres arthropodes, mais la transmission par griffure reste le mode principal reconnu.
Transmission :
La transmission à l’être humain se fait principalement :
- par contact oculaire ou cutané avec des mains souillées après manipulation d’un animal infecté
- par griffure ou morsure de chat
Incubation et symptômes :
Après une griffure ou une morsure, l’incubation est généralement d’une à trois semaines.
Les manifestations les plus fréquentes sont :
- une petite lésion cutanée au point d’inoculation (papule, pustule ou croûte)
- une adénopathie régionale (ganglion augmenté de volume, souvent douloureux)
- des symptômes généraux modérés : fièvre, fatigue, céphalées, douleurs musculaires
La maladie touche plus fréquemment les enfants et les adolescents, mais peut survenir à tout âge. Dans la majorité des cas chez les personnes immunocompétentes, l’évolution est spontanément favorable.
Facteurs de risque :
Les facteurs favorisant la transmission incluent :
- la présence de puces chez le chat
- des jeux favorisant griffures ou morsures
- une désinfection insuffisante des plaies
Chez les personnes immunodéprimées, des formes plus sévères peuvent survenir.
Articles sur le sujet :
- Page Ameli du 23.04.2025
- CENTER FOR DISEASE CONTROL AND PREVENTION. 2015. Bartenolla Infection (Cat Scratch Disease, Trench Fever, and Carrion’s Disease) >
- LYME DISEASE – Lyme Disease Co-infection: Bartonella >
- CHOMEL.B.B., KASTEN.R.W. 2010. Bartonellosis, an increasingly recognized zoonosis >
- Symptômes de la Bartonelle. Human Bartonellosis: An Underappreciated Public Health Problem? >
- Bartonellose chez des patients présentant des disfonctions neurologiques et neurocognitives >
5. La fièvre Q
La fièvre Q est une zoonose causée par la bactérie Coxiella burnetii. Elle est présente dans de nombreuses régions du monde, y compris en France. Les principaux réservoirs sont les ruminants domestiques (bovins, ovins, caprins).
Contrairement aux maladies principalement transmises par les tiques, la voie de contamination la plus fréquente chez l’être humain est l’inhalation de particules contaminées (aérosols) provenant de sécrétions, de déjections ou de produits de mise bas d’animaux infectés. La transmission par piqûre de tique est possible chez l’animal mais demeure exceptionnelle chez l’être humain.
Transmission :
La contamination humaine se fait principalement :
• par inhalation de poussières contaminées
• par contact direct avec des animaux infectés ou leurs produits biologiques
• plus rarement par ingestion de produits laitiers non pasteurisés
La transmission interhumaine est exceptionnelle.
Incubation :
La période d’incubation varie généralement de 2 à 3 semaines après l’exposition.
Manifestations cliniques :
La fièvre Q peut se présenter sous différentes formes cliniques. La forme aiguë associe le plus souvent :
- fièvre élevée
- frissons
- céphalées intenses
- fatigue marquée
- douleurs musculaires
Des atteintes pulmonaires (pneumonie atypique) ou hépatiques (hépatite) peuvent survenir. Un rash cutané est possible mais inconstant.
Dans la majorité des cas, l’évolution est favorable sous traitement adapté. Une convalescence prolongée avec fatigue persistante peut être observée.
Une forme chronique, rare mais potentiellement grave, peut se développer chez certaines personnes à risque, notamment sous la forme d’une endocardite ou d’une infection vasculaire.
Facteurs de risque :
Les principaux facteurs de risque sont :
- l’exposition professionnelle aux élevages (agriculteurs, vétérinaires, personnels d’abattoirs)
- le contact avec des animaux en période de mise bas
- la proximité d’exploitations agricoles
- certaines pathologies cardiaques ou vasculaires préexistantes (pour les formes chroniques)
- l’immunodépression
La fièvre Q est probablement sous-diagnostiquée en raison de la variabilité de ses manifestations cliniques et de leur caractère souvent peu spécifique.
6. La méningo-encéphalite à tiques
La méningo-encéphalite à tiques (MET), également appelée encéphalite à tiques, est une infection virale du système nerveux central causée par le virus TBEV (Tick-Borne Encephalitis Virus), un arbovirus transmis principalement par les tiques du genre Ixodes.
Transmission :
La transmission à l’être humain se fait principalement :
- par la piqûre de tiques infectées
- plus rarement par ingestion de lait cru ou de produits au lait cru provenant d’animaux infectés (chèvres, brebis, plus rarement vaches)
La transmission interhumaine n’est pas décrite.
Incubation :
La période d’incubation est généralement comprise entre 7 et 14 jours après la piqûre, mais peut varier de 2 à 28 jours.
Manifestations cliniques :
La maladie évolue souvent en deux phases :
Première phase (virémique)
Elle se manifeste par un syndrome pseudo-grippal :
- fièvre
- fatigue
- céphalées
- douleurs musculaires
Cette phase peut durer quelques jours et être suivie d’une amélioration transitoire.
Seconde phase (neurologique)
Chez une proportion des patients, une atteinte du système nerveux central survient secondairement, pouvant se traduire par :
- méningite
- encéphalite
- méningo-encéphalite
- troubles neurologiques (troubles de la conscience, paralysies, troubles de l’équilibre)
Des séquelles neurologiques persistantes peuvent être observées dans certaines formes sévères.
La létalité des formes européennes est généralement estimée entre 0,5 % et 2 %, selon les données disponibles.
Il n’existe actuellement aucun traitement antiviral spécifique ; la prise en charge est symptomatique et hospitalière dans les formes neurologiques.
Facteurs de risque :
Les principaux facteurs de risque sont :
- l’exposition aux tiques dans les zones d’endémie
- les activités en milieu forestier ou rural
- la consommation de lait cru provenant d’animaux infectés
En Europe, la maladie est plus fréquente en Europe centrale, orientale et nordique. En France, des cas autochtones ont été signalés, notamment dans l’Est du pays et plus récemment dans d’autres régions, ce qui suggère une extension géographique progressive.
Prévention :
La prévention repose sur :
- les mesures de protection contre les piqûres de tiques
- la consommation de produits laitiers pasteurisés
- la vaccination dans les zones d’endémie ou pour les personnes exposées
Un vaccin contre l’encéphalite à tiques est disponible et utilisé dans plusieurs pays européens.
Données réglementaires :
La méningo-encéphalite à tiques n’est pas actuellement une maladie à déclaration obligatoire en France.
Elle ne figure pas, à ce jour, dans les tableaux des maladies professionnelles.
Le virus TBEV est classé comme agent biologique du groupe 3 au sens du Code du travail. Cette classification signifie qu’il s’agit d’un agent infectieux pouvant provoquer une maladie grave chez l’être humain et présenter un risque pour les travailleurs exposés, mais pour lequel des mesures de prévention et de protection existent.
7. Les arbovirus
Les arboviroses sont des maladies virales causées par des arbovirus, c’est-à-dire des virus transmis par des arthropodes comme les tiques ou les moustiques. En France, plusieurs arboviroses transmises par les tiques ont été identifiées. La plus connue est l’encéphalite à tiques européenne, transmise principalement par Ixodes ricinus, et considérée comme la plus significative en termes de santé publique.
D’autres arbovirus circulent plus discrètement, notamment dans des zones fréquentées par des oiseaux migrateurs, qui peuvent jouer un rôle de réservoir. Ces infections sont des zoonoses, c’est-à-dire des maladies transmises à l’être humain à partir d’animaux vertébrés par l’intermédiaire d’un vecteur.
8. Les rickettsioses
Les rickettsioses sont des infections causées par des bactéries du genre Rickettsia, de très petite taille, appartenant à l’ordre des Rickettsiales. De nombreuses espèces ont été identifiées, dont certaines sont responsables de maladies humaines. La majorité de ces bactéries est transmise par des arthropodes, principalement des tiques, mais aussi parfois des puces ou des acariens. Les tiques peuvent à la fois servir de vecteur et de réservoir.
En France métropolitaine, plusieurs espèces de Rickettsia circulent, notamment dans le pourtour méditerranéen, où certaines rickettsioses sont endémiques. Toutefois, le pouvoir pathogène de certaines espèces identifiées chez les tiques reste encore mal caractérisé.
La période d’incubation est généralement de 6 à 10 jours. La maladie débute le plus souvent par un syndrome fébrile brutal associant fièvre élevée, céphalées intenses, douleurs musculaires et articulaires, parfois accompagnées de nausées ou de vomissements. Une lésion cutanée au point de piqûre, appelée escarre d’inoculation (ou « tache noire »), peut apparaître et constitue un élément d’orientation diagnostique important. Une éruption cutanée maculeuse peut également se développer secondairement.
Dans l’expérience des patients, les symptômes initiaux sont souvent décrits comme particulièrement intenses, avec une fatigue marquée et un état général altéré pouvant entraîner une consultation en urgence. Comme les signes cliniques sont peu spécifiques au début, le diagnostic peut être retardé si l’exposition aux tiques ou le séjour en zone d’endémie n’est pas identifié. Le diagnostic repose en premier lieu sur les données cliniques et épidémiologiques (saison, exposition, voyage, activité professionnelle, contact avec des animaux).
En l’absence de traitement adapté, des complications peuvent survenir, notamment chez les personnes fragiles. Un traitement antibiotique précoce permet en général une évolution favorable.
9. La tularémie
La tularémie est une maladie infectieuse causée par la bactérie Francisella tularensis, un bacille aérobie particulièrement résistant dans l’environnement. Le principal réservoir est constitué par les lièvres, les lapins et divers rongeurs, mais la bactérie peut infecter de nombreuses autres espèces animales.
Transmission :
La transmission à l’être humain peut se faire :
- par contact direct avec un animal infecté (manipulation de gibier, chasse)
- par contact avec un environnement ou des objets contaminés
- par inhalation de poussières contaminées
- par ingestion d’eau ou d’aliments contaminés
- par la piqûre d’arthropodes vecteurs, notamment certaines tiques, mais aussi plus rarement des taons ou d’autres insectes hématophages
La transmission interhumaine n’est pas décrite.
Incubation :
La période d’incubation est généralement courte, le plus souvent de 3 à 5 jours, mais peut aller jusqu’à deux semaines.
Manifestations cliniques :
L’apparition des symptômes est souvent brutale, avec :
- fièvre élevée
- frissons
- céphalées intenses
- fatigue marquée
- douleurs musculaires
Selon la voie de contamination, différentes formes cliniques peuvent être observées :
forme ulcéro-ganglionnaire (avec ulcération au point d’inoculation et ganglions régionaux), forme ganglionnaire isolée, forme oculo-ganglionnaire, forme pulmonaire ou forme typhoïdique plus générale.
Le tableau clinique peut être variable, ce qui peut rendre le diagnostic difficile en l’absence de notion d’exposition.
Facteurs de risque :
Les principaux facteurs de risque sont :
- les activités de chasse et de manipulation de gibier
- les professions exposées (agriculteurs, forestiers, vétérinaires)
- l’exposition aux tiques en zone rurale ou forestière
- la manipulation d’animaux sauvages
Données réglementaires :
La tularémie est une maladie à déclaration obligatoire en France.
Elle figure également dans les tableaux des maladies professionnelles (n°68 du régime général et n°7 du régime agricole).
Articles sur le sujet :
- La tularémie >
- Étude française (AP-HP Henri-Mondor) sur la tularémie >
- Les maladies du gibier, Hélène Thiboutot >
10. L’ehrlichiose / l’anaplasmose
Les ehrlichioses regroupent un ensemble d’infections zoonotiques comprenant l’ehrlichiose humaine et animale ainsi que l’anaplasmose humaine. Elles sont causées par des bactéries intracellulaires du genre Ehrlichia et Anaplasma, transmises le plus souvent par la piqûre de tiques.
Ces agents infectent principalement certaines cellules du système immunitaire et provoquent généralement un syndrome fébrile aigu associant fièvre, céphalées, fatigue et douleurs musculaires. En l’absence de traitement adapté, des complications peuvent survenir, notamment chez les personnes fragiles. »
11. Allergie alimentaire émergente à l’alphagal
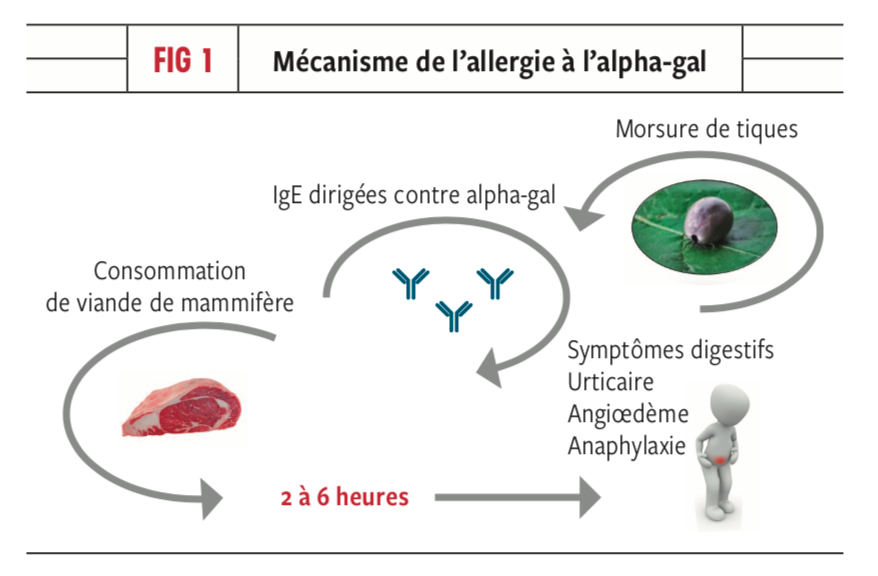
L’allergie à l’alpha-gal est une réaction allergique particulière déclenchée par un sucre appelé galactose-α-1,3-galactose (alpha-gal). Ce sucre est présent dans les tissus des mammifères (bovins, ovins, porcins, gibier), mais absent chez les poissons et les volailles.
Certaines piqûres de tiques peuvent induire une sensibilisation à l’alpha-gal. Lors du repas sanguin, la tique injecte des substances issues d’animaux mammifères précédemment piqués, ce qui peut déclencher chez certaines personnes une réponse immunitaire inadaptée. Après cette sensibilisation, la consommation de viande rouge ou de produits dérivés de mammifères peut provoquer une réaction allergique.
Cette allergie se distingue par son caractère retardé : les symptômes apparaissent généralement 3 à 6 heures après l’ingestion, souvent au cours de la nuit. Les manifestations peuvent aller d’urticaire et de troubles digestifs à des réactions plus sévères, incluant un choc anaphylactique.
L’allergie à l’alpha-gal est désormais reconnue comme une cause importante d’anaphylaxie chez l’adulte, notamment après 60 ans. Le diagnostic repose sur l’interrogatoire, le contexte d’exposition aux tiques et la mise en évidence d’anticorps spécifiques.
Quelques articles sur le sujet :
- 2018 Avis de l’Anses Allergie Alpha galactose >
- 2023 Allergie alimentaire émergente à l’alphagal – D A Moneret-Vautrin, professeur émérite Faculté de Médecine de Nancy >
- CDC Alpha-gal syndrome en français >
- 10 faits nouveaux et surprenants sur le syndrome de l’alpha-Gal >
12. Le virus Alongshan
Le virus Alongshan est un virus transmis par les tiques, identifié pour la première fois en Chine, près de la ville d’Alongshan. Les infections décrites se manifestent principalement par de la fièvre, des maux de tête, de la fatigue et parfois des nausées. Les données restent encore limitées et les connaissances sur sa répartition géographique et son impact clinique continuent d’évoluer.
- 2022, des tiques suisses sont porteuses du récent virus Alongshan
- 2019, A New Segmented Virus Associated with Human Febrile Illness in China
13. La fièvre hémorragique de Crimée-Congo
La fièvre hémorragique de Crimée-Congo (FHCC) est une maladie virale causée par un virus du genre Nairovirus, transmis principalement par des tiques du genre Hyalomma. Elle peut provoquer une fièvre brutale accompagnée de troubles hémorragiques dans ses formes sévères. Le taux de létalité varie selon les contextes sanitaires, généralement estimé entre 10 et 40 %.
La maladie est endémique dans certaines régions d’Afrique, des Balkans, du Moyen-Orient et d’Asie. En Europe, des cas humains ont notamment été signalés en Espagne. En France, des tiques Hyalomma sont présentes dans le sud du territoire, mais aucun cas autochtone humain n’a été rapporté à ce jour.
- ANSES, article en ligne de 2024, La fièvre hémorragique de Crimée-Congo, un risque d’émergence en France
- Article de Le Parisien de 2024, un homme contaminé par une tique en Espagne
- AVIS et RAPPORT de l’Anses relatif à l’analyse des risques pour la santé humaine et animale liés aux tiques du genre Hyalomma en France
- Haut Conseil de la santé publique, avis 2024, Prévention et prise en charge de la fièvre hémorragique Crimée-Congo
14. « Virus des zones humides », le Wetland Virus en anglais (WELV)
Le virus des zones humides (Wetland Virus, WELV) est un virus identifié en Chine et appartenant au genre Orthonairovirus. Il est transmis par certaines tiques. Des études menées dans le nord de la Chine ont détecté sa présence chez un faible pourcentage de tiques analysées. Les données disponibles restent limitées et les connaissances sur son impact chez l’être humain sont encore en cours d’étude.
15. Virus Powassan
Le virus de Powassan est un virus transmis par les tiques, principalement présent en Amérique du Nord, notamment au Canada et dans certaines régions des États-Unis. La maladie de Powassan est rare mais peut être grave lorsqu’elle entraîne une atteinte neurologique.
La transmission peut survenir rapidement après la piqûre de tique. La période d’incubation varie généralement de 1 à 4 semaines. Les premiers symptômes sont souvent non spécifiques et peuvent ressembler à un syndrome grippal, avec fièvre, céphalées et fatigue.
Où sont présents les agents infectieux transmis par les tiques en France ?
La répartition des agents infectieux transmis par les tiques en France est variable selon les régions, les espèces de tiques et les réservoirs animaux. Les données disponibles proviennent de travaux de surveillance épidémiologique, d’études de recherche et des réseaux de veille sanitaire.
Santé publique France, l’ANSES et plusieurs équipes de recherche publient régulièrement des données sur la circulation des tiques et des pathogènes associés. La Haute Autorité de Santé a également synthétisé les connaissances disponibles dans ses recommandations actualisées relatives à la borréliose de Lyme et aux autres maladies vectorielles à tiques. Voir les Recommandations HAS 2025 pages 11 à 22 (épidémiologie et agents infectieux en France).
Il convient de noter que les connaissances évoluent régulièrement, certaines régions étant mieux étudiées que d’autres, et que la présence d’un agent infectieux dans une tique ne signifie pas nécessairement un risque identique pour l’ensemble du territoire.
Les co-infections
La borréliose de Lyme est due à des bactéries du complexe Borrelia burgdorferi sensu lato et constitue la maladie transmise par les tiques la plus fréquemment diagnostiquée en France. Toutefois, les tiques peuvent héberger et transmettre simultanément plusieurs agents infectieux.
Outre Borrelia, d’autres bactéries, parasites ou virus peuvent être inoculés lors d’une même piqûre de tique, notamment Anaplasma phagocytophilum, certaines espèces de Rickettsia, des bactéries du genre Ehrlichia, Francisella tularensis, des parasites du genre Babesia, ainsi que le virus de l’encéphalite à tiques. La fréquence réelle de ces co-transmissions varie selon les régions, les espèces de tiques et les réservoirs animaux.
Le terme « maladies vectorielles à tiques » (MVT) désigne l’ensemble des infections transmises à l’être humain par l’intermédiaire d’un vecteur, en l’occurrence la tique. Le mot « vectoriel » renvoie précisément à cette notion de transmission par un organisme intermédiaire.
On parle de co-infection lorsqu’une personne est infectée par plusieurs agents pathogènes transmis lors d’une même exposition ou de piqûres successives. La présence de plusieurs agents infectieux peut parfois modifier la présentation clinique, influencer l’intensité des symptômes ou compliquer l’interprétation diagnostique. Néanmoins, chaque situation doit être évaluée individuellement par un médecin, en fonction du contexte clinique et épidémiologique.
La recherche scientifique se poursuit afin de mieux comprendre la fréquence réelle de ces co-infections et leur impact sur l’évolution des maladies transmises par les tiques.
